The Telegraph rapporterade nyligen att allmänheten har blivit tillsagd att sluta ta mediciner mot hosta och förkylningar på grund av säkerhetsrädslor angående drogen, folkodin, ett opioidhostdämpande medel.
Tjugo av de vanliga host- och förkylningsläkemedlen, inklusive Day- och Night Nurse-kapslar, har omedelbart dragits tillbaka från marknaden på order av läkemedelsmyndigheterna på grund av oro över en "mycket sällsynt" risk för anafylaxi, en livshotande biverkning.
Tillkännagivandet "Class 2 Medicines Recall" hämtat från den brittiska regeringens webbplats, visas nedan.

När det gäller mRNA COVID-19-vaccinerna har de reglerande dubbla standarderna aldrig varit så uppenbara.
Anafylaxi identifierades som en viktig risk av European Medicines Agency, redan i december 2020, i EMA:s CHMP (Committee for Medicinal Products for Human Use) utvärderingsrapport om Pfizer-BioNTech COVID-19-vaccinet, se nedan.
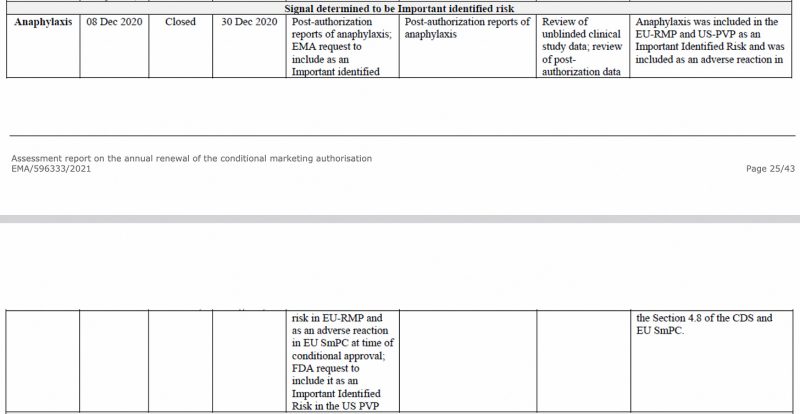
Dessutom i EU:s första periodiska säkerhetsuppdatering Rapport, som jag har tidigare analyseras, anafylaxi flaggades återigen som en viktig identifierad risk.

I denna farmakovigilansrapport identifierades 3,827 XNUMX relevanta fall (individer) utifrån data efter godkännandet. Landet med högst incidens var Japan, följt av USA och Storbritannien.
Det högsta antalet rapporterade fall var bland kvinnor, chockerande 3,182 454 fall jämfört med 44 fall för män, med en medianålder på 7. Att 2021 gånger fler fall rapporterades för kvinnor är inget nytt. Tillbaka i december XNUMX, I analyseras Pfizer förberedd dokumentera för FDA, som täcker 3-månadersperioden, december 2020 till och med 28 februari 2021 – i fallet med anafylaxi – var kvinnor 8 gånger mer drabbade.
Så, 98 procent av de relevanta biverkningarna (inklusive anafylaktisk reaktion, anafylaktisk chock, anafylaktoid reaktion och anafylaktoid chock) klassificerades som allvarliga!
Dessutom, för 92 procent av händelserna, var tiden som gick innan en biverkning inträffade efter vaccinadministrering mindre än 24 timmar.

Dödliga utfall
Av de 3,922 28 händelserna var 704 dödliga och för svindlande XNUMX var resultatet okänt. Inga fallnummer gavs för dödliga utfall.

Fall efter åldersgrupp
Av de 3,827 23 relevanta fallen (individer) var 3,021 från den pediatriska åldersgruppen och XNUMX XNUMX från den vuxna åldersgruppen.
Förekomst av samsjukligheter
Vad som är anmärkningsvärt är att ungefär 2/3 av alla anafylaxifall gjorde det inte har några samsjukligheter (underliggande hälsoproblem).

Med tanke på vad som har hänt sedan mRNA COVID-19-vaccinerna rullades ut, kommer det inte som någon överraskning att läsa: "ingen ny säkerhetsinformation identifierades relaterade till risken för anafylaxi med BNT162b2” (Pfizer-BioNTech COVID-19-vaccin). Anledningen (eller ursäkten de gömmer sig bakom) är att "denna risk kommuniceras... som inkluderar information om lämpliga åtgärder som ska vidtas, enligt följande: "Som med alla injicerbara vacciner måste lämplig medicinsk behandling och övervakning alltid vara lätt tillgänglig i händelse av en sällsynt anafylaktisk händelse efter administrering av vaccinet."
Enligt Förordning 174, Information för brittisk sjukvårdspersonal, som senast reviderades i december 2021, står följande:

n faktum, på själva första dagen av Pfizer-BioNTech COVID-19-vaccinutrullningen i Storbritannien, fanns det två rapporter om anafylaxi och ett rapporterat fall av en möjlig allergisk reaktion. Detta hindrade inte MHRA från att återkalla produkten – de kringgick helt enkelt problemet genom att säga att personer som har en historia av allergier inte borde ta vaccinet.
Även när de visste- Pfizer/BioNTechs lipidnanopartikelingredienser ALC-0159 och ALC-0315 har aldrig inkluderats i något licensierat läkemedel tidigare. ALC-0159 innehåller PEG (polyetylenglykol) vilket är känt för att orsaka anafylaxi.
Det är otvetydigt: anafylaxi var en känd livshotande biverkning, ungefär samtidigt som tillstånd för akut användning beviljades för Pfizer-BioNTech COVID-19-vaccinet. Men eftersom det är ett "injicerbart vaccin" har det på något sätt fått ett frikort från alla läkemedelsregulatorer, oavsett hur mycket fördömande data som ackumuleras, när en hostsaft eller kapsel å andra sidan brådskande återkallas på grundval av en "a mycket sällsynt risk för anafylaxi."
Återpublicerad från författarens understapel
Publicerad under a Creative Commons Erkännande 4.0 Internationell licens
För omtryck, vänligen ställ tillbaka den kanoniska länken till originalet Brownstone Institute Artikel och författare.









